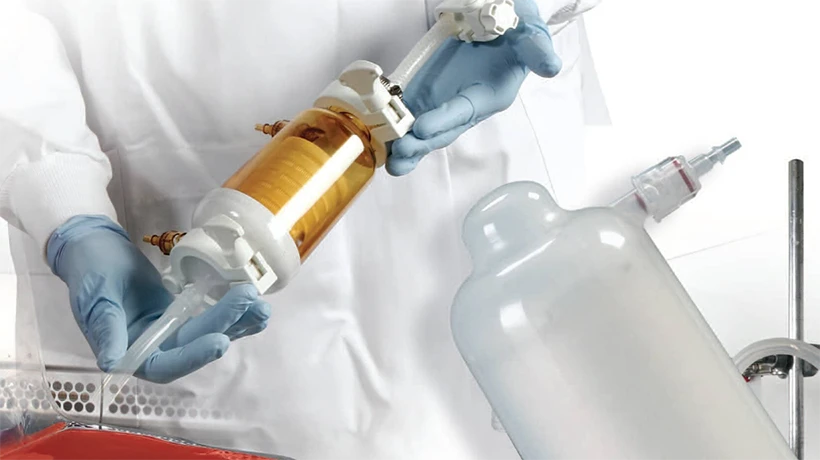
Il processo di test e verifica può garantire che prodotti come i filtri pieghevoli forniscano prestazioni accurate e affidabili nell'ambiente industriale e siano conformi agli standard e alle specifiche delle apparecchiature sanitarie nazionali ed estere.
- Casa
- Prodotti

Forniamo un servizio di approvvigionamento one-stop per materiali filtranti di grado sanitario e accessori, riducendo i costi di approvvigionamento.
Leggi di più - Industrie

Siamo specializzati nella fornitura di prodotti e servizi di filtrazione per l'industria microelettronica, biofarmaceutica e alimentare e delle bevande con elevate esigenze igieniche.
Leggi di piùIndustrie - Garanzia di qualità

La qualità è la nostra missione ed è nostro dovere garantire che i nostri prodotti soddisfino le richieste del settore.
Leggi di piùGaranzia di qualità - Conoscenza

Fornire linee guida per la selezione dei prodotti e servizi di conoscenza tecnica per ridurre i costi di selezione.
Leggi di piùConoscenza - A proposito

Benvenuto, siamo un fornitore globale di mezzi di filtrazione sanitari e accessori, specializzato nella fornitura di soluzioni sanitarie di filtrazione.
Leggi di piùA proposito - Contatto