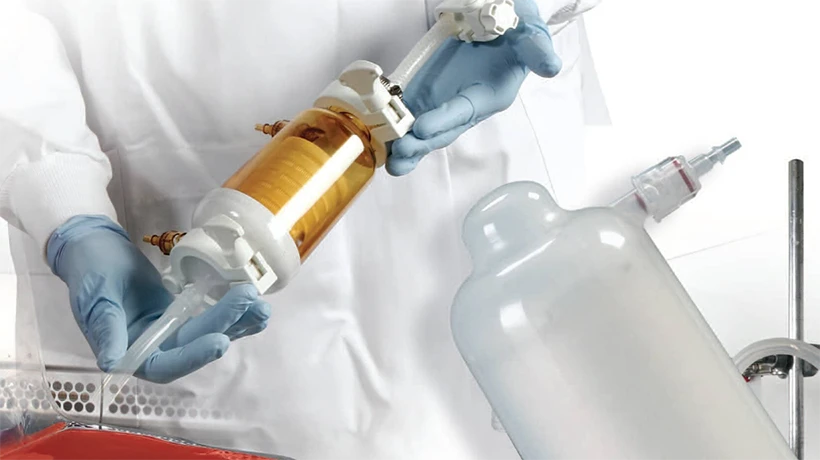
Le processus de test et de vérification peut garantir que des produits tels que les filtres pliants offrent des performances précises et fiables dans l'environnement de l'industrie, et sont conformes aux normes et spécifications des équipements sanitaires nationaux et étrangers.
- Accueil
- Produits

Nous fournissons un service d'approvisionnement unique pour les matériaux et les accessoires de filtre de qualité sanitaire, réduisant vos coûts d'approvisionnement.
Lire plus - Industries

Nous sommes spécialisés dans la fourniture de produits et de services de filtration pour la microélectronique, les produits biopharmaceutiques et les industries alimentaires et des boissons ayant des besoins élevés en matière d'hygiène.
Lire plus - Assurance qualité

La qualité est notre mission et il est de notre devoir de nous assurer que nos produits répondent aux exigences de l'industrie.
Lire plusAssurance qualité - Connaissance

Fournir des directives de sélection de produits et des services de connaissances techniques pour réduire vos coûts de sélection.
Lire plusConnaissance - À propos de

Bienvenue, nous sommes un fournisseur global des médias et des accessoires sanitaires de filtration, se spécialisant en fournissant les solutions sanitaires de filtration.
Lire plusÀ propos de - Contact